 Yaşam
Yaşam
 Yemek
Yemek
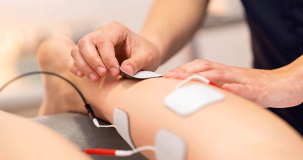 Sağlık
Sağlık
 Moda ve Güzellik
Moda ve Güzellik
 Faydalı Bilgiler
Faydalı Bilgiler
 Eğitim
Eğitim
 Doğa ve Hayvanlar
Doğa ve Hayvanlar
Elektrokimyasal pil , kimyasal enerjiyi elektrik enerjisine dönüştüren düzeneklerdir. 1800 yılında A. Volta ve 1870 yılında L. Galvani, birbirinden habersiz olarak ilk kez kimyasal enerjiyi elektrik enerjisine çeviren hücreler yapmışlardır. Bu tür pillere Volta pili veya Galvani pili denir
Faraday elektroliz yasaları , 1834 yılında Michael Faraday tarafından yayımlanan, elektroliz olayındaki madde-elektrik ilişkisini açıklayan elektrokimya yasalarıdır
Faraday'ın elektroliz yasalarının iki temel ilkesi :
Elektroliz , istemsiz kimyasal bir tepkimenin elektrik enerjisiyle gerçekleştirilmesi işlemidir. Elektroliz, elektrolitik hücrelerde gerçekleştirilir
Elektrokimyasal dengede katot daha aktiftir, çünkü indirgemenin gerçekleştiği elektrottur ve elektronları dış devreden alır.
Hayır, Amper yasası ve Faraday yasası aynı değildir. Ampere yasası, manyetik alanın elektrik akımı yoluyla üretilmesini anlatır. Faraday yasası ise manyetik alandaki değişikliğin elektrik alan meydana getirdiğini belirtir. Her iki yasa da Maxwell denklemlerinin bir parçasıdır.
Elektrokimyasal pillerde elektrot potansiyellerinin farkı, aşağıdaki faktörlere bağlıdır: 1. Elektrot Cinsi: Farklı elektrot türleri kullanıldığında hücre potansiyeli değişir. 2. Sıcaklık: Sıcaklık artışı, pil geriliminin azalmasına neden olur. 3. Derişim: Yarı hücrelerdeki çözeltilerin derişimlerinin değişmesi, elektrokimyasal hücre potansiyelini etkiler. 4. Basınç (gazlar için): Sadece SHE içeren galvanik pillerde basınç değişimi potansiyeli etkiler. Ayrıca, standart elektrot potansiyelleri, elektrotların yükseltgenme veya indirgenme eğilimlerine göre de belirlenir.
Elektrokimyasal pillerde (galvanik hücreler) anot elektrotta yükseltgenme, katot elektrotta ise indirgenme reaksiyonları gerçekleşir. Anot. Katot.
Elektrokimyasal pillere günlük hayattan örnekler şunlardır: 1. Alkalin Piller: Televizyon kumandaları, oyuncaklar ve dijital kameralar gibi cihazlarda kullanılır. 2. Lityum Piller: Dizüstü bilgisayarlar, cep telefonları ve elektrikli araçlarda tercih edilir. 3. Çinko-Hava Piller: İşitme cihazlarında ve kan şekeri ölçüm cihazlarında kullanılır. 4. Gümüş Oksit Piller: Kol saatleri ve ana kart yedek pilleri olarak kullanılır. 5. Düğme Piller: Saatler, hesap makineleri ve küçük dijital termometreler gibi düşük güç gerektiren cihazlarda bulunur.
Elektrokimyasal pillerde gerilim (pil potansiyeli) hesabı, E0hücre = E0ind(katot) – E0ind(anot) veya E0hücre = E0ind(katot) – E0yük(anot) formülleriyle yapılır. Bu formüllerde: E0hücre, standart hücre potansiyelini; E0ind, standart indirgenme potansiyelini; anot ve katot, yarı hücrelerde gerçekleşen tepkimeleri ifade eder. Ayrıca, ΔE°pil = E°(katot) - E°(anot) formülü de kullanılabilir. Elektrotların cinsi, çözelti derişimleri ve sıcaklık gibi faktörler pil potansiyelini etkiler.
Elektrokimyasal pillerde elektrolit olarak çeşitli tuzların doymuş çözeltileri (örneğin, KNO3, KCl) ve asidik çözeltiler (örneğin, 1 M H+ iyonu içeren asit çözeltisi) kullanılabilir. Ayrıca, sirkeli su gibi asetik asit içeren çözeltiler de elektrolit olarak kullanılabilir. Elektrolit, elektriksel yüklerin taşınmasını sağlayan çözeltidir.
 Eğitim
Eğitim
E-okul diploma kayıt örneği veriyor mu?
Duyusal bellek ve duyusal kayıt aynı şey mi?
Edirne neden İstanbul'dan önce başkent oldu?
En eski papirüs hangi Mısır'da bulundu?
Dünya'da en çok hangi maden var?
Ekvator neden sıcak?
En derin sondaj kaç km?
Editoryal çalışma nasıl yapılır?
Egmod sınavında kaç soru var?
Elastik ve esnek aynı şey mi?
Ek puan kimlere verilir meb?
Dünya gezegenler arasında kaçıncı sırada?
EBA şifresi nasıl alınır?
E okula eksi not girilirse ne olur?
E-okul diploma sorgulama nasıl yapılır?
Elementler doğada poliatomik bulunabilir mi?
DYK kurs başvurusu nasıl sorgulanır?
Elma suyu asit mi baz mı?
Elektrik alan nedir?
Elektrik manyetizma en zor konu mu?
En iyi KPSS bölümü hangisi?
En kötü barış en haklı savaştan iyidir sözü kime ait?
Emevi Devleti'nin kuruluş ve yıkılış tarihi nedir?
Ege Üniversitesi Eğitim Fakültesi hangi kampüste?
Ekstremum nokta için türev şart mı?
Elektrik alanın şiddeti nelere bağlıdır?
En güçlü kuvvetten en zayıf kuvvete doğru sıralama nasıl yapılır?
Ekop açılımı nedir?
Dünyada ilk kağıt fabrikası nerede kuruldu?
Elektron katman dağılımı grup ve periyotu verir mi?
Dünyanın ağırlığı ve havanın ağırlığı aynı mı?
Eksiden eksi çıkarsa artı olur mu?
Dünya'nın yörüngesi neden elips?
E-okul mezun öğrenci belgesi nasıl alınır?
En tehlikeli yakıcı madde nedir?
Ebonite çubuk yün kumaşa sürtüldüğünde nasıl yüklenir?
Edebiyat geçme notu 70 ne zaman geçerli?
E okulda devamsızlık girişi ne zaman kapanır?
E portfolyo nasıl hazırlanır?
Elmas, grafit ve fullerenin ortak özellikleri nelerdir?